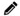
Titre
Pourquoi
Le laboratoire doit tirer profit de toute non-conformité. En agissant après détection de chaque non-conformité selon un processus qui suit le cycle planifier, réaliser, vérifier, ajuster, une amélioration continuelle peut automatiquement être obtenue.
Quoi
Une non-conformité est un événement qui n'est pas conforme aux règles et/ou aux attentes. Comme exemples, on peut citer des écarts par rapport aux paramètres critiques environnementaux ou caractérisant l'équipement, des accidents, des échantillons incorrectement conditionnés, des ruptures de stock, etc. Dans la colonne de droite figure un lien vers un document tiré du manuel Système de gestion de la qualité au laboratoire (LQMS) de l'OMS présentant des informations sur la gestion des non-conformités (appelé "Gestion des problèmes" dans le manuel LQMS).
Rédiger une POS relative à la gestion des non-conformités. Les annexes à cette POS sont le formulaire de non-conformité et la liste de pointage.
Pour éliminer les non-conformités d'une manière qui débouche sur une amélioration continue, la procédure suivante doit être exécutée :
- Enregistrer chaque non-conformité sur un formulaire de non-conformité standardisé. Dans la colonne de droite, figure un lien vers un modèle de formulaire de ce type. Ce formulaire doit présenter de bonnes instructions car une non-conformité peut être notifiée par n'importe quel membre du personnel ; d'abord la non-conformité doit être décrite, y compris ses causes possibles. La personne qui notifie la non-conformité doit également indiquer son nom sur le formulaire. Sur le formulaire doit figurer l'instruction "Remettre ce formulaire au responsable du laboratoire".
- Le responsable du laboratoire doit ensuite faire ce qui suit :
- Estimer la gravité des conséquences de la non-conformité et l'indiquer sur le formulaire.
- Faire une analyse pour étudier ce qui a provoqué la non-conformité. Pour cela, le responsable du laboratoire doit demander l'aide de la personne responsable de l'unité du laboratoire dans laquelle la non-conformité est survenue et le responsable du laboratoire peut demander à la personne qui a notifié la non-conformité de participer à la réflexion.
- Formuler des actions correctives et des actions préventives basées sur les observations de l'analyse des causes pour éliminer la non-conformité et l'empêcher de se reproduire à l'avenir. Si nécessaire et possible, des étapes de contrôle doivent également être formulées pour savoir si la non-conformité se reproduit.
- La mise en œuvre en temps voulu des actions correctives et préventives et des étapes de contrôle doit être formulée en actions à mener selon la méthode SMART sur le formulaire de non-conformité, indiquant dans quel délai (en fixant une date butoir) la non-conformité doit être éliminée/corrigée et le(s) nom(s) de la (des) personne(s) qui doit (doivent) mettre en œuvre les actions à mener.
- En-dessous de la section dans laquelle sont écrites les actions à mener, le responsable du laboratoire doit indiquer si l'efficacité des actions correctives et préventives nécessite une évaluation. Sur le formulaire figure ensuite l'instruction "Remettre ce formulaire au responsable qualité".
- Le responsable du laboratoire doit discuter de la non-conformité, y compris les façons de l'éliminer/la corriger, lors d'une réunion hebdomadaire du personnel. Les personnes chargées de la mise en œuvre des actions à mener doivent être averties.
- Lorsqu'il reçoit le formulaire, le responsable qualité doit inclure les actions à mener dans les comptes rendus de la réunion hebdomadaire du personnel pour surveiller et garantir leur mise en œuvre. Si le responsable du laboratoire a indiqué que l'efficacité des actions préventives et correctives devait être évaluée, le responsable qualité doit établir une liste de pointage des non-conformités (voir ci-dessous).
- Le responsable qualité ne doit pas archiver le formulaire tant que l'exécution des actions à mener n'est pas achevée. Lorsque toutes les actions à mener ont été mises en œuvre, le formulaire de non-conformité doit être signé et daté par le responsable du laboratoire et ensuite archivé dans un nouveau classeur intitulé "Non-conformités".
Il est important qu'un formulaire de non-conformité soit rempli pour chaque non-conformité identifiée. Chaque membre du personnel doit en être conscient car chacun peut contribuer à l'amélioration des services du laboratoire. Pour inciter le personnel à l'enregistrement systématique des non-conformités sur les formulaires, il est essentiel que ceux-ci restent simples et puissent être remplis rapidement par la personne qui notifie la non-conformité.
Une liste de pointage peut être utilisée pour déterminer l'efficacité des actions correctives et préventives introduites après des non-conformités constatées dans le passé. Dans ce cas, on établit une liste décrivant la non-conformité à éliminer/corriger. Dans la colonne de droite, figure un lien vers un modèle de liste de ce type. Ces listes peuvent être placées en un endroit accessible pour tous les membres du personnel, par exemple le tableau d'affichage. Lors d'une réunion hebdomadaire, informer les membres du personnel de l'existence de ces nouvelles listes et leur demander de pointer les non-conformités quand ils en détectent. Si, après la mise en œuvre d'actions correctives et préventives, des non-conformités continuent d'être enregistrées sur la liste de pointage par les membres du personnel, le responsable du laboratoire saura que les actions correctives et préventives n'ont pas été totalement efficaces.
Les listes de pointage sont également très utiles pour détecter une augmentation de la fréquence des non-conformités. Par exemple : Les formulaires de demande ne sont pas toujours bien remplis. Il est trop fastidieux de remplir un formulaire de non-conformité chaque fois que cela se produit. Dans ce cas, le laboratoire peut utiliser une liste sur laquelle la non-conformité sera pointée au moment où elle survient.
Comment & qui
Responsable qualité, en concertation avec le responsable du laboratoire :
- Formuler la description ci-dessus en une POS relative à la gestion des non-conformités. Suivre le protocole de rédaction d'une POS relative aux procédures dans la POS-cadre et utiliser le modèle de POS relative aux procédures joint à la POS-cadre.
- Réviser et valider la POS selon la POS relative au contrôle des documents.
- Lorsque la POS est finalisée et en vigueur, l'ajouter dans la liste Lu et Compris et signaler que tous les membres du personnel doivent la lire.
- Présenter la POS lors d'une réunion hebdomadaire du personnel. Expliquer aux membres du personnel l'importance de l'enregistrement de chaque non-conformité, comment est exécutée la procédure d'élimination/correction des non-conformités et leur indiquer comment utiliser les formulaires de non-conformité et les listes de pointage. Expliquer où les membres du personnel peuvent trouver des formulaires de non-conformité vierges.
- Vérifier si les membres du personnel commencent à notifier et consigner les non-conformités. Si aucun formulaire de non-conformité rempli n'est reçu, insister à nouveau sur l'importance de l'enregistrement des non-conformités lors d'une réunion hebdomadaire du personnel, jusqu'à ce que cette démarche porte ses fruits.
Responsable du laboratoire :
- Adapter la grille d'autorisation pour inclure les tâches et responsabilités décrites dans la POS relative à la gestion des non-conformités pour les différents postes dans le laboratoire.