Titre
Pourquoi
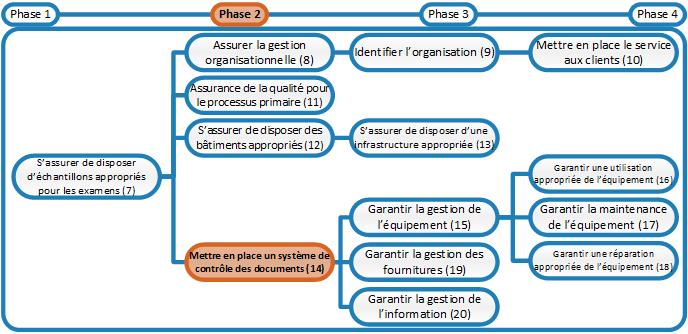
En phase 2, a été établi le système de contrôle des documents garantissant une révision régulière des documents relatifs à la gestion de la qualité (POS, manuel des services du laboratoire, chapitres du manuel de la qualité et chapitres du manuel de sécurité biologique avec toutes leurs annexes et tous leurs formulaires). De cette manière, l'exactitude de la documentation utilisée dans la pratique du laboratoire est assurée, ce qui est un facteur de l'assurance de la qualité. Pour garantir que le système de contrôle des documents reste fonctionnel et que toutes les procédures en lien avec le contrôle des documents sont toujours effectuées de manière correcte, complète et identique, le système de contrôle des documents doit également être standardisé.
Quoi
Élaborer une POS pour le contrôle des documents. Dans cette POS, toutes les procédures en lien avec le contrôle des documents établies en phase 2 doivent être documentées :
- Ajouter de nouveaux documents au registre de contrôle des documents.
- Actualiser le registre de contrôle des documents lorsqu'une nouvelle version d'un document est mise en circulation (voir l'activité relative à l'élaboration d'un registre de contrôle des documents).
- Examen des documents selon le calendrier (voir l'activité relative à l'élaboration du système de contrôle des documents).
- Examiner les documents, de manière planifiée (révision d'un document selon le calendrier prévu) ou non planifiée (détection d'une erreur dans un document qui doit être corrigée immédiatement) (voir l'activité sur l'élaboration d'un formulaire de révision de document).
- Remplacer les anciennes versions des documents par les nouvelles versions des documents dont la mise en circulation a été autorisée : veiller à ce que toutes les anciennes copies soient remplacées par de nouvelles copies et qu'une copie de l'ancienne version de la POS conservée en archive soit datée et étiquetée "remplacée" (voir l'activité relative à l'élaboration du système de contrôle des documents). Toutes les autres copies seront détruites.
- Trier les archives du laboratoire pour retirer les documents qui peuvent être détruits parce que la durée maximale d'archivage est atteinte, comme indiqué dans la liste d'archivage des documents.
Comment & qui
Responsable qualité :
- Rédiger la POS relative au contrôle des documents selon le protocole de rédaction d'une POS relative aux procédures décrite dans la POS-cadre. Utiliser le modèle d'une POS relative aux procédures joint à la POS-cadre. Ajouter la liste d'archivage des documents élaborée précédemment en phase 2 comme annexe de cette POS.
- Faire réviser et valider la POS selon la procédure décrite dans la POS-cadre.
- Déterminer en quels endroits des copies de cette POS doivent être conservées et indiquer ces endroits sur la première page avec en-tête de la POS (comme cette POS n'est destinée qu'au responsable qualité et, le cas échéant, aux gestionnaires des documents, il peut être suffisant de conserver une copie de cette POS dans la zone des bureaux et dans les archives des documents relatifs à la qualité).
- Imprimer la POS et la distribuer dans les endroits indiqués sur la première page avec en-tête.
- Déterminer qui doit lire cette POS : toutes les parties de cette POS ne sont pas importantes pour tous les membres du personnel. Cependant, la procédure destinée aux révisions non planifiées des documents en cas de détection d'une erreur concerne tous les membres du personnel et ils devraient avoir connaissance de cette procédure et être capables d'agir en fonction de celle-ci. Ajouter cette POS à la liste Lu et Compris et indiquer qui doit lire la POS.
- Faire une présentation du système de contrôle des documents lors d'une réunion hebdomadaire du personnel et expliquer pourquoi il a été établi et comment il fonctionne. Présenter la POS relative au contrôle des documents durant la même réunion et indiquer quels membres du personnel doivent la lire et quelle(s) section(s) ils doivent lire.
- Surveiller la mise en œuvre correcte des procédures selon la POS.

